ラムナン硫酸の抗SARS-CoV-2活性
他グループの研究ではありますが、興味深い結果が報告されたので紹介します。(DOI: 10.3390/md19120685)
新型コロナウイルス感染症(COVID‑19)の原因である新型コロナウイルスとして知られるSARS-CoV-2(重症急性呼吸器症候群コロナウイルス2)は、自身のスパイクタンパク質(図1参照)を生体細胞の表面に存在するACE2(アンジオテンシン変換酵素2:タンパク質の一種)に結合することで、細胞内に侵入することが知られています。また、この際に同じく生体細胞表面に存在するヘパラン硫酸(多糖の一種)などの糖鎖がウイルスの結合を補助していることが示唆されています(図1参照)。
これまでの研究で、フコイダンなどの硫酸化多糖がSARS-CoV-2感染阻害作用を示すことを報告してきましたが、今回硫酸化多糖の一種であるラムナン硫酸のSARS-CoV-2感染阻害作用について調べました。その結果、分子レベルの実験においてラムナン硫酸は、濃度依存的にスパイクタンパク質とヘパラン硫酸の一種であるヘパリンとの結合を阻害しました(図2参照)。また、ラムナン硫酸は細胞レベルの実験において疑似SARS-CoV-2の感染を阻害しました(図3参照)。これらは、疑似SARS-CoV-2のスパイクタンパク質がヘパラン硫酸と結合する際に、同じ硫酸化多糖であるラムナン硫酸がヘパラン硫酸と競合的にスパイクタンパク質に結合するためと考えられました(図4参照)。
今回の結果から、ラムナン硫酸はSARS-CoV-2感染予防物質の候補となりうることが示唆されました。今後さらなる研究が期待されます。
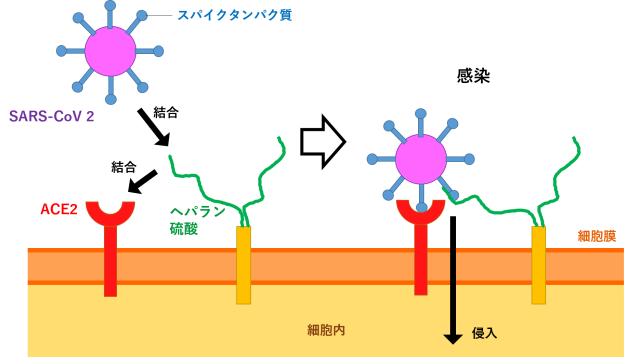
図1 SARS-CoV-2の感染にはACE2との結合が必要ですが、その際にヘパラン硫酸が結合を補助していると考えられています。
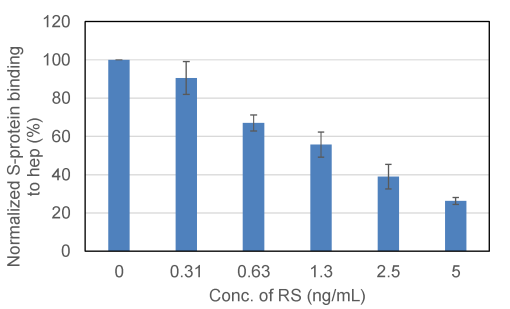
図2 縦軸はスパイクタンパク質とヘパリンとの結合率、横軸はラムナン硫酸の濃度を表しています。ラムナン硫酸の濃度依存的にスパイクタンパク質とヘパリンの結合率が低下しています。(図は論文より転載)
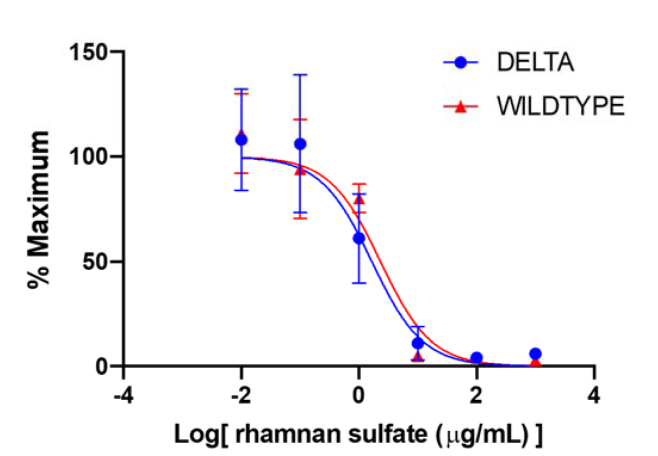
図3 縦軸は感染率、横軸はラムナン硫酸の濃度(対数値)を表しています。ラムナン硫酸の濃度依存的に感染率が低下しています。また、DELTAはデルタ株(変異株)、WILDTYPEは野生型(非変異株)を示しており、どちらにも同等の効果が見られました。(図は論文より転載)
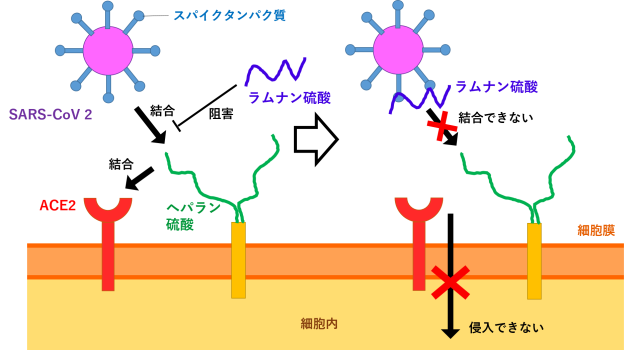
図4 SARS-CoV-2がヘパラン硫酸と結合する際に、ラムナン硫酸が存在するとヘパラン硫酸と類似構造のため競合的にスパイクタンパク質と結合し、感染が阻害されると考えられています。
以下のページに論文の和訳(一部)を記載しました。

